某医疗器械有限公司内部审核检查表(DOC 40页)
所属分类:内部审计
文件大小:418 KB
下载要求:10 学币或VIP
点击下载
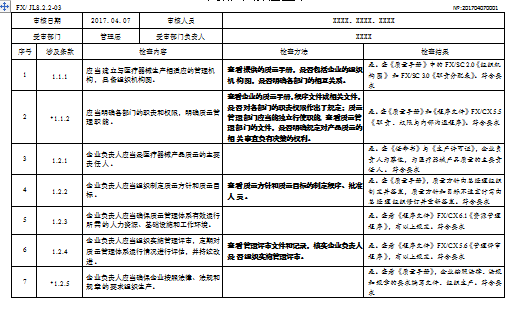
11.1.1应当建立与医疗器械生产相适应的管理机构,具备组织机构图。
查看提供的质量手册,是否包括企业的组织机构图,是否明确各部门的相互关系。
是。查《质量手册》中的FX/SC2.0《组织机构图》和FX/SC3.0《职责分配表》。符合要求
1.应当包括更改对产品组成部分和已交付产品的影响;
1.应当在设计和开发过程中开展设计转换活动以解决可生产性、
部件及材料的可获得性、所需的生产设备、操作人员的培训等;
1.应当在适宜阶段进行设计和开发确认,确保产品满足规定的使用要求或预期用途的要求;
1.应当按设计开发策划的结果,在适宜的阶段进行设计和开发评审;
1.应当结合策划的结果,在适宜的阶段进行设计和开发验证,确保设计开发输出满足输入的要求;
1.设计和开发的各个阶段的划分;
1.设计和开发项目的目标和意义的描述,技术指标分析;
1.采购信息,如原材料、包装材料、组件和部件技术要求;
1.风险管理应当覆盖企业开发的产品实现的全过程
..............................
下一篇:内部审核检查表(DOC 38页)
精品资料网 m.cnshu.cn
Copyright © 2004- 粤ICP备10098620号-1
